AVITI의 높은 염기 정확도와 데이터 퀄리티는 RCA(Rolling Circle Amplification) 기반의 PCR-free 증폭과 Avidity Chemistry에서 비롯됩니다. AVITI는 라이브러리를 원형화(circularization)하여 플로우셀 표면에서 RCA로 직접 폴로니(polony)를 형성하므로, PCR 증폭 과정에서 유래한 오류가 연쇄적으로 증폭되는 문제를 근본적으로 억제합니다. 그 결과 템플릿 오류의 전파가 감소하고, Optical duplication과 amplification에서 유발된 index hopping 같은 artifact도 줄어듭니다(그림. 1). 이는 브리지 증폭에 의존하는 시퀀싱 방식과 대비되는 특징입니다. 실제 비교 연구에서도 AVITI 시퀀싱은 기존 SBS 기반 장비 대비 유의하게 낮은 오류율과 더 높은 read 퀄리티 스코어를 보여주었습니다.
Avidity 기반 시퀀싱은 형광 염료로 표지된 코어(dye-labeled core)에 여러 개의 뉴클레오타이드 리간드가 다가결합(multivalent binding)을 형성하도록 설계하여, 폴리머레이스–폴리머–뉴클레오타이드 복합체가 polony에 매우 안정적으로 결합하도록 합니다. 이 다가결합은 리포팅 뉴클레오타이드의 필요 농도를 마이크로몰(μM)에서 나노몰(nM) 수준으로 낮추고 해리율을 유의하게 줄여, 신호 대비 잡음 비율을 개선하면서 동일 염기서열에 대해 강하고 선명한 신호를 제공합니다.
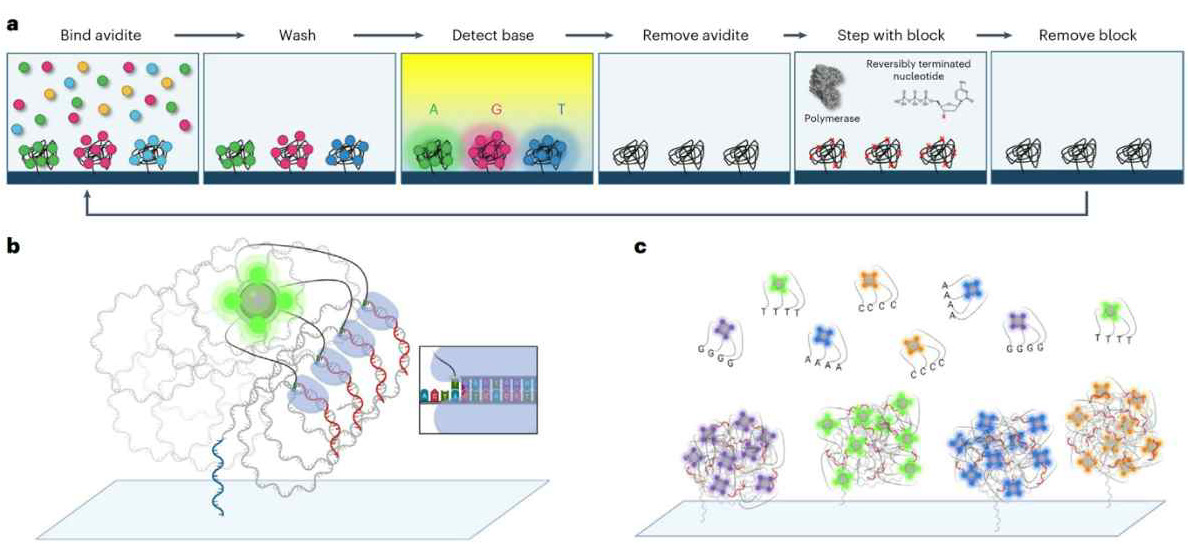 <그림 1> Avidity sequencing workflow and scheme
<그림 1> Avidity sequencing workflow and scheme
각 이러한 화학적·광학적 이점을 통해 AVITI는 동일 성능을 더 적은 시약으로 달성할 수 있으며, 이는 운영 비용 절감으로 직결됩니다. 또한 Avidity 기반 시퀀싱이 높은 정확도(Qscores)와 호모폴리머 구간에서의 안정적 오류 프로파일, 그리고 시약 소비 절감 효과를 동시에 얻을 수 있습니다.
Q40 시퀀싱이 제시하는 새로운 기준: 더 높은 정확도로 비용을 절감하고 희귀 변이 검출을 향상시키는 방법 제시
NGS 기술의 발전은 임상 연구의 가능성을 다시 정의하고 있습니다. 암 연구자들은 난이도 높은 샘플에서도 검출 수준을 높여 미세잔존질환(MRD) 및 조기 내성 발생의 모니터링을 위해 노력하고 있으며, 이때 시퀀싱 데이터의 정밀도와 신뢰성이 무엇보다 중요해지고 있습니다.
지금까지 NGS 플랫폼은 Q30(99.9% 정확도) 수준의 결과를 제공해 왔으며, coverage depth의 향상과 오류 수정 기법의 발전을 통해 다양한 응용이 가능해졌습니다. 최근 들어 NGS의 근본적인 기술력 향상으로 Q40 시퀀싱(99.99% 정확도)이 등장하면서 품질이 비약적으로 향상되었고, 이러한 원시 데이터의 정확도의 상승이 변이 검출에 어떤 영향을 미치는지에 대한 관심이 높아졌습니다.
푸단대학교(Fudan University)의 최근 연구는 지금까지 발표된 연구 중에서도 Q40 시퀀싱을 DNA 및 RNA 시퀀싱 모두에 걸쳐 가장 포괄적으로 탐구한 사례 중 하나입니다(그림. 2). 연구진은 Element Biosciences의 AVI-TI™ 시스템을 이용해 Q40 데이터를 생성하고, 이를 기존 Q30 결과와 비교하여, 임상적으로 중요한 희귀 변이의 검출 능력이 향상됨으로써 시퀀싱 비용이 절감될 수 있음을 입증했습니다.
민감도, 정밀도, 비용 효율성이 핵심인 전임상 및 임상 종양학 연구 분야에서 이러한 결과는 저빈도 체세포 돌연변이를 탐지하고 질병의 진행도를 추적하기 위한 시퀀싱 데이터 활용 방식의 중대한 발전을 의미합니다.
연구진은 시퀀싱 정확도의 향상이 downstream 분석 정밀도에 미치는 영향을 평가하기 위해 대조 샘플 세트(reference standard set)를 사용하여 다양한 검증을 진행했습니다.
1. 생식세포 변이 분석(Germline variant calling precision): NIST RM 8398 표준의 전장 엑솜 시퀀싱(whole exome sequencing)을 이용해 변이 검출 정밀도를 평가했습니다.
2. 멘델 일관성(Mendelian consistency): Quartet control 세트를 이용해 확인했습니다.
3. RNA 검출 및 발현 정량 분석: MAQC 샘플과 ERCC 합성 스파이크인 풀을 포함한 잘 특성화된 RNA controls로부터 생성된 bulk RNA-seq 데이터를 활용했습니다.
4. 체세포 변이 검출 정확도(Accuracy of somatic variant detection): HCC1295/BL 혼합 reference 샘플을 사용했습니다.
비교를 위해 동일한 샘플을 Element Biosciences AVITI와 Illumina NovaSeq 6000 플랫폼에서 시퀀싱했으며, 공정한 성능 비교를 위해 모든 데이터셋은 동일한 커버리지 수준으로 다운샘플링 되었습니다.
생식세포 변이 분석 결과, AVITI 데이터셋에서 더 낮은 중복률(duplication rate)을 관찰했으며, 이는 이전에 보고된 Avidite Base Chemistry™의 특성과 일치하는 결과였습니다. 그러나 단순히 중복률 감소만으로 향상된 결과를 모두 설명할 수는 없었습니다.
핵심적인 발견은 10×에서 120×까지 다운샘플링된 커버리지 수준에서 InDel 및 SNV 정확도를 비교했을 때 나타났습니다. AVITI Q40 데이터는 Illumina Q30 데이터와 동일한 수준의 정확도를 단 66.6%의 상대적 커버리지로 달성했습니다.
연구진은 이러한 효율성 향상이 가지는 실질적 의미를 강조하며, 시퀀싱 depth 필요량의 감소는 응용 분야에 따라 샘플당 약 30~50%의 비용 절감 효과로 이어질 수 있음을 시사했습니다.
유전 질환 연구와 대규모 인구 집단 연구에서는 생식계열 변이의 높은 정확도가 필수적이지만, 연구진은 Q40 시퀀싱 정확도의 가장 혁신적인 영향은 종양학 분야, 특히 희귀 체세포 변이의 탐지에서 나타날 수 있음을 언급했습니다. 이를 평가하기 위해, 저빈도 돌연변이(low frequency mutations)를 모사한 대조 샘플을 사용하여 AVITI Q40 시퀀싱과 Illumina Q30 시퀀싱의 성능을 비교했습니다. 생식계열 변이 분석 결과와 일관되게, AVITI는 훨씬 낮은 시퀀싱 커버리지만으로 동일한 민감도와 정밀도를 달성하는 데 충분하다는 점이 보고되었습니다. 또한 낮은 커버리지 수준에서도 복제수 변이(CNV) 탐지 성능이 유의미하게 향상됨이 관찰되었습니다.
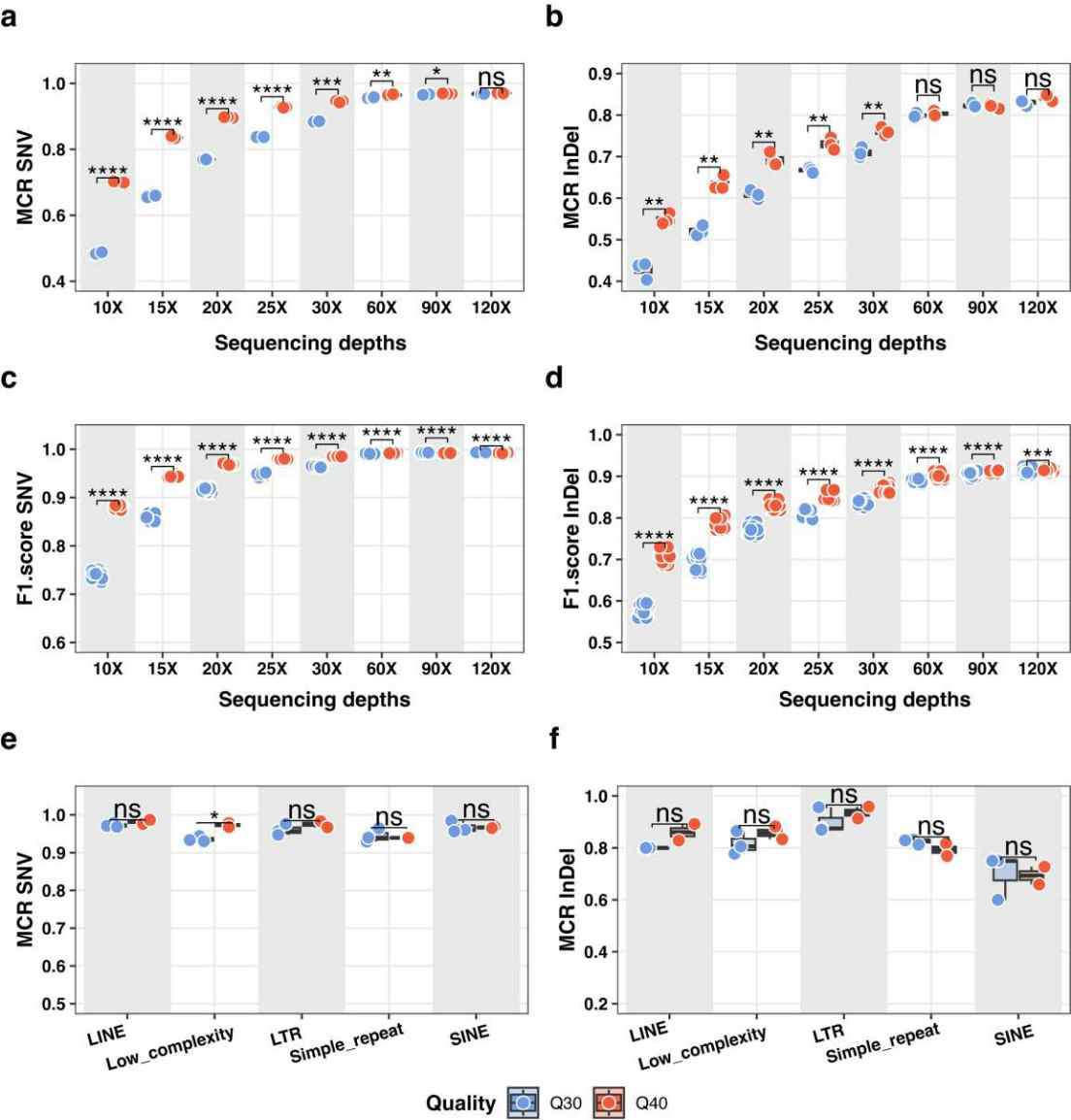 <그림 2> Germline SNV and InDel calling performance (Q30 vs. Q40).
<그림 2> Germline SNV and InDel calling performance (Q30 vs. Q40).
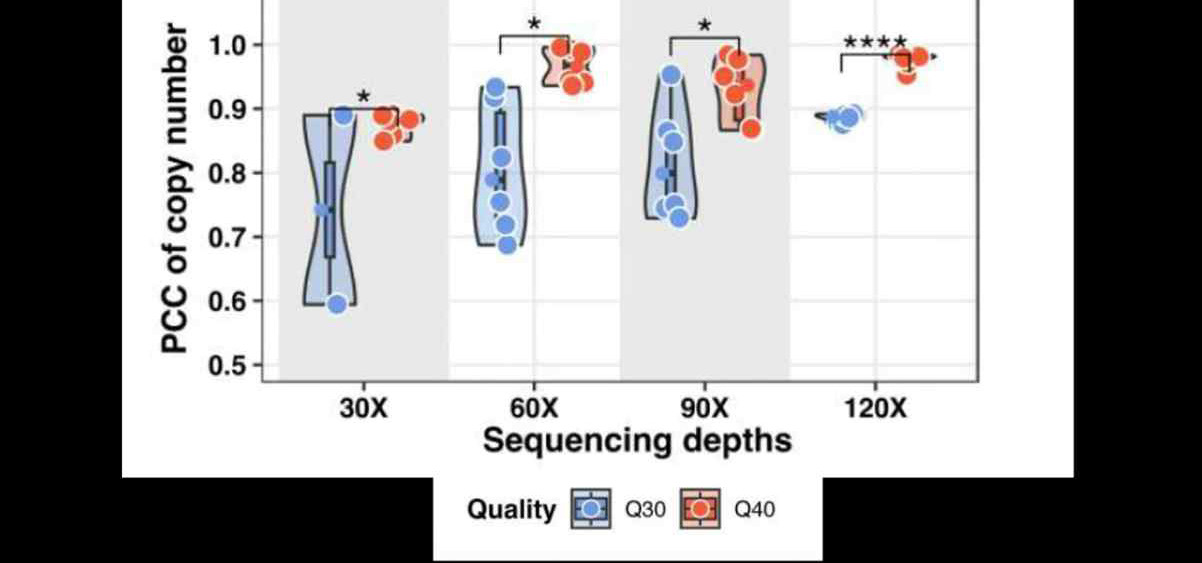 <그림 3> Somatic CNV calling performance (Q30 vs Q40)
<그림 3> Somatic CNV calling performance (Q30 vs Q40)
이러한 연구 결과의 중요성은 최소 침습을 통해 종양 유래 DNA를 검출하려는 액체생검(liquid biopsy)의 지속적인 발전으로 더욱 커지고 있습니다. 종양학 분야의 응용이 변이 대립유전자 빈도(variant allele frequency, VAF) 0.1% 이하를 목표로 하게 되면서, 시퀀싱 민감도에 대한 요구 수준은 점점 더 높아지고 있습니다. 현재의 방법들은 시퀀싱 노이즈를 억제하고 탐지 정확도를 향상시키기 위해 UMI(unique molecular identifiers)에 크게 의존하지만, 약 1:1000 수준의 낮은 변이 빈도를 신뢰성 있게 검출하기 위해 필요한 분자 및 alignment coverage를 확보하려면 매우 높은 시퀀싱 depth가 필요합니다. 이는 샘플당 비용을 크게 증가시키고 응용 확장성을 제한합니다.
AVITI의 높은 염기 정확도는 이러한 한계를 극복할 새로운 방향을 제시합니다. 원시 리드(raw read)의 정확도가 높아지면, 각 UMI당 훨씬 적은 수의 리드만으로도 신뢰도 높은 consensus 서열을 생성할 수 있게 되어 전체 시퀀싱 요구량과 비용을 모두 줄일 수 있습니다. 연구진은 이러한 시퀀싱 정확도의 향상이 액체생검 기술을 연구 단계 이상의 일상적 임상 검사 적용으로 확장시키는 핵심 요인이 될 수 있다고 평가합니다.
해당 분야에서의 지속적인 혁신은 임상 연구에서의 고성능 시퀀싱 기술의 채택을 한층 더 가속화할 것으로 예상됩니다. Element Biosciences는 최근 UltraQ™ 화학 기술을 통해 Q50 이상의 시퀀싱 성능을 구현하며 정확도 면에서의 기술적 리더십을 확장했습니다. 향후 민감도, 확장성, 비용 효율성의 지속적인 향상은 초고정확도 시퀀싱을 종양학 및 기타 정밀의학 응용 전반에서 폭넓게 활용하기 위한 중요한 역할을 하게 될 것입니다.
임상 유전체 분야는 ‘정확성’, ‘속도’, ‘멀티오믹스’라는 세 가지 축에서 빠르게 진화하고 있습니다. AVITI 시스템은 높은 처리량과 개선된 에러 프로파일, 그리고 AVITI24가 제시하는 빠른 멀티오믹스·공간분석 워크플로우를 통해 임상 진단과 연구를 잇는 가교 역할을 할 수 있습니다. 구체적으로는 (1) 희귀질환의 삼자(Trio) WGS 워크플로우 최적화, (2) 액체생검·저빈도 변이 모니터링의 민감도 향상, (3) 종양 미세환경 기반 프로파일링을 통한 맞춤치료 마커 발굴 등에서 현장에서 요구하는 가치를 제공할 수 있을 것으로 기대됩니다.
[References]
1. Arslan, S., Garcia, F. J., Guo, M., et al. (2024). Sequencing by avidity enables high accuracy with low reagent consumption. Nature Biotechnology, 42(1), 132–138. https://doi.org/10.1038/s41587-023-01750-7
2. Duan, S., Liu, Y., Guo, X., et al. (2025). Q40 sequencing reduces costs and enhances detection of low-frequency somatic variants (Version 1). Research Square. https://doi.org/10.21203/rs.3.rs-7283107/v1

