결핵균(Mycobacterium tuberculosis, MTB) 감염은 공중 보건 분야에서 여전히 중대한 난제 중 하나로 여겨지며 특히 치료제 내성 및 HIV 동반 감염이 문제시되고 있습니다. OECD 회원국 중 발생률과 사망률 모두 최하위로 [1] 우리나라의 결핵 발생자 수는 꾸준히 줄어들고 있지만, 2019년도에도 30,000명 이상의 환자가 발생하였습니다. [2] 2021년 WHO의 새로운 보고에 의하면 다약제내성 결핵(Multi drug-resistant tuberculosis)환자가 매년 470,000건에 달하는 것으로 나타나고 있습니다. [3]
결핵퇴치협력네트워크(Stop Tuberculosis Partnership)에서는 2030년을 목표로 인구 100,000명당 20건 미만으로 결핵의 종말이라는 WHO의 목표를 달성하고자 결핵퇴치(END tuberculosis) 전략을 글로벌 계획에 (Global Plan)에 착수했습니다. 결핵 퇴치를 위해서는 기존 사고방식의 전환, 새로운 진단 전략, HIV와 결핵 진단 서비스 간의 상호 통합이 요구될 것입니다. [4]

cobas®MTB는 cobas 6800 system(체외 수인 15-1087 호) 및 cobas 8800 system(체외 수인 15-1087 호)을 이용하여, 불활성화된 원(raw) 객담, 불활성화된 용해-오염제거(N-acetyl-L- cysteine/NaOH [NALC-NaOH]-처리된) 객담 및 기관지 폐포 세척(bronchoalveolarlavage: BAL) 검체를 포함한 항산균(acid-fast bacilli: AFB) 도말-양성 또는 도말-음성인 불활성화된 사람의 호흡기 검체에서 결핵균 복합체(Mycobacterium tuberculosis complex: MTBC) DNA 를 직접 검출하기 위해 실시간 중합효소연쇄반응(real-time polymerase chain reaction: PCR)으로 정성하는 자동화된 체외진단 의료기기입니다. [5]
cobas®MTB검사는 결핵균(Mycobacterium tuberculosis) 감염이 의심되고 항결핵요법을 받지 않고 있는 환자 검체가 대상이며, 임상징후, 배양 및 기타 검사 결과와 함께 폐결핵 진단을 돕기 위해 사용됩니다. [5]
cobas®MTB는 분석 전 검체 액화 및 mycobacteria 불활성화 후 검체 초음파 처리 및 완전 자동화된 검체 준비(핵산 추출 및 정제), PCR 증폭 및 검출을 기반으로 합니다. 검체 액화 및 mycobacteria 불활성화는 cobas Microbial Inactivation Solution (MIS)으로 검체를 배양하는 동안 동시에 일어납니다. 액화 및 불활성화된 검체의 초음파 처리는 cobas 6800/8800 system 에 장착하기 전에 수행됩니다. cobas 6800/8800 system 은 검체 공급 모듈, 이동 모듈, 처리 모듈 및 분석 모듈로 구성되어 있습니다. 자동화된 데이터 관리가 cobas 6800/8800 소프트웨어에 의해 수행되어 모든 검사에 대해 검사 결과를 양성, 음성 또는 무효로 부여합니다. 결과는 장비 화면에서 직접 확인할 수 있으며 외부로 보내거나 보고서를 출력할 수 있습니다. [5]
 Figure 1. 검체의 전처리 Automation
Figure 1. 검체의 전처리 Automation
핵산은 환자 검체 및 외부 대조물질, 첨가된 내부 대조물질 DNA (DNA-IC) 분자에서 동시에 추출됩니다. 요약하면, 박테리아의 핵산은 화학적(cobas Microbial Inactivation Solution (MIS), cobas omni Lysis Reagent), 효소적(proteinase) 및 물리적(초음파처리)인 박테리아 분쇄에 의해 방출됩니다. 방출된 핵산은 첨가된 자성유리입자(magnetic glass particles)의 실리카 표면에 결합합니다. 비결합 물질과 변성단백질, 세포파편, 잠재적인 PCR 저해제 등의 불순물들은 다음 세척단계에서 제거되고 정제된 핵산은 상승된 온도에서 elution buffer 로 자성유리입자에서 분리됩니다. 검체로부터 타깃 핵산의 선택적인 증폭은, 각각의 타깃 유기체 내 매우 보존적인 부분(conserved region)으로부터 선택된 MTB 복합체를 위한 타깃-특이적 정방향 및 역방향 프라이머를 사용하여 이루어집니다. [5]
MTB 는 선택적인 두 세트의 프라이머와 별개의 영역(이중 타깃(dual-target), 16S rRNA gene 및 esx genes - esxJ, esxK, esxM, esxP, 및 esxW)을 표적으로 하는 2 개의 프로브에 의해 검출됩니다. DNA IC 의 선택적인 증폭은 MTB 복합체 타깃 부위와 상동성(homology) 없는 것으로 선택된 서열-특이적 정방향 및 역방향 프라이머를 사용하여 이루어집니다. 내열성 DNA polymerase 효소가 PCR 증폭에 사용됩니다. 타깃 및 DNA-IC 서열은 온도 단계 와 사이클 수가 미리 지정된 범용 PCR 증폭 profile 을 이용하여 동시에 증폭됩니다. Master mix 는 deoxythimidine triphosphate(dTTP) 대신 deoxyuridine triphosphate(dUTP)가 들어있으며, 이는 새로 합성되는 DNA(amplicon)에 삽입됩니다. 이전 PCR 검사에서 오염된 amplicon 이 있을 경우 PCR master mix 에 들어있는 AmpErase 효소에 의해 첫 번째 thermal cycling 단계에서 제거됩니다. 그러나 AmpErase 효소가 일단 55℃이상의 온도에 노출되면 불활성화되기 때문에 새로 형성된 amplicon 은 파괴되지 않습니다. [5]
cobas®MTB의 master mix 는 MTB 복합체 타깃 서열에 특이적인 2 개의 검출 프로브와 DNA-IC 에 대한 1 개의 검출 프로브를 포함하고 있습니다. 타깃 특이적 프로브는 두 곳의 타깃 채널에서 MTB 복합체 타깃과 DNA IC 가 동시에 검출될 수 있도록 각기 다른 형광 리포터 염료로 표지되어 있습니다. 타깃 서열에 결합되지 않으면, 손상되지 않은 프로브(intact probe)의 형광 시그널은 quencher 염료에 의해 억제됩니다. PCR 증폭 단계에서, 특이적인 한가닥 DNA 템플릿(specific single-stranded DNA template)에 프로브가 hybridization 되면 DNA polymerase 의 5' -> 3' exonuclease 활성에 의한 프로브의 cleavage 로 인해 리포터와 quencher 염료가 분리되고 형광 시그널이 생성됩니다. 각 PCR cycle 과 함께, 생성되는 cleaved 프로브가 증가하고 부수적으로 리포터 염료의 누적 시그널이 증가합니다. PCR 제품의 실시간 검출 및 식별은 MTB 복합체 타깃 및 DNA-IC 에 대해 방출된 각각의 리포터 염료의 형광을 측정하여 이루어집니다. [5]
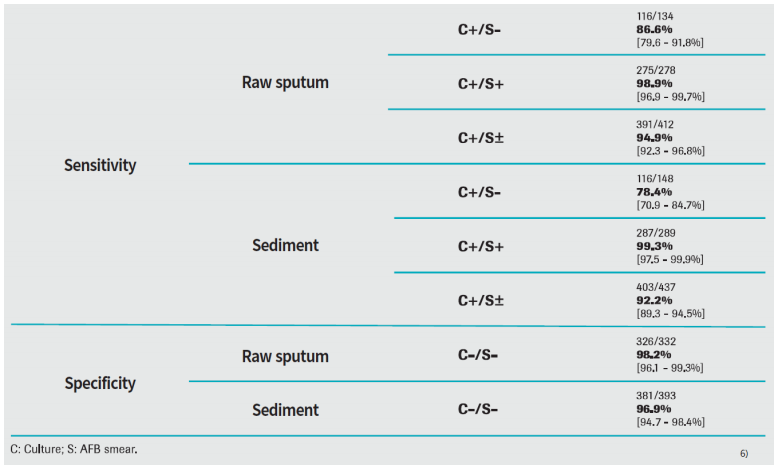 Table1. 실제 임상검체로 확인된 cobas®MTB의 민감도 및 특이도
Table1. 실제 임상검체로 확인된 cobas®MTB의 민감도 및 특이도
[참고문헌]
[1] Social Welfare Review (http://dx..doi.org/10.15709/hswr.2017.37.4.179)
[2] 질병관리본부_2019 결핵환자_신고현황_연보
[3] World Health organization, Multidrug-resistant tuberculosis (MDR-TB): 2021.
(https://www.who.int/news/item/27-01-2021-who-announces-updated-definitions-of-extensively-drug-resistant-tuberculosis)
[4] Stop TB Partnership. The paradigm shift 2016-2020: Global plan to end TB; 2015. (http://www.stoptb.org/global/plan/plan2/. Last accessed August 2018)
[5] cobas®MTB Package Insert
[6] Method sheet “cobas® MTB”
[허가사항]
[1] cobas MTB 체외 수허 19-305호
[2] cobas 6800_8800 체외 수인 15-1087호

