차세대염기서열분석법(NGS)는 2017년 NGS 유전자패널 검사가 선별급여로 보험 적용된 이후 현재 총 63기관에서 시행되고 있습니다. NGS 유전자패널 검사의 고형암 분야는 2019년 한차례 개정을 통해 전체 암종으로 확대됨과 동시에, 인정 기준을 초과한 고형암 검사 분야는 검사비 90% 환자부담으로 허용되었습니다. 이러한 보험 제도의 변화는 고형암 환자를 대상으로 액체생검을 적용할 수 있는 시금석이 되었습니다.
액체생검은 세계 선도적인 NGS 전문업체 Illumina(CA, USA)사의 패널과 플랫폼을 기반으로 진단 시장이 개척되었으며, 많은 국내 panel 제조사와 연구소등에서도 전용 패널과 분석툴 개발을 서둘러 출시하였습니다. 검사 단가가 높으며 보다 정밀한 분석을 수행해야 하는 NGS 기반 액체생검은 run마다 검사가 원활하게 진행되는지 판단할 수 있는 과정이 필요합니다. 이에 QC물질 전문기업 LGC Seracare사는 액체생검용 정도관리물질 제품을 출시하였습니다.
LGC Seracare사의 정도관리물질은 국내 panel 제조사의 개발 과정에 reference material로 사용된 바 있습니다.
1. 액체생검은 조직검사의 실패율과 제한점을 보완할 수 있습니다. 암 발생부위에서 누출된 circulating tumor DNA (ctDNA)는 온 몸을 순환하기 때문에, 조직검사 검체 채집시 발생하는 지엽적 실패를 방지합니다. 종양 내 이질성(Tumor heterogeneity)은 반복적인 조직검사를 강요하는 주된 실패 요인입니다. 표적치료제의 biomarker 발견을 전제하는 동반진단의 검사방법으로 조직검사보다 액체생검이 더 효과적입니다.
NCCN 임상 진료 가이드라인에서는 1) Non-Small Cell Lung Cancer, 2) Breast Cancer, 3) Esophageal and Esophagogastric Junction Cancers, 4) Gastric Cancer, 5) Prostate Cancer, 6) Pancreatic Adenocarcinoma, 7) Histiocytic Neoplasms 등 7 종에 대하여 액체생검의 사용을 권고하고 있습니다.
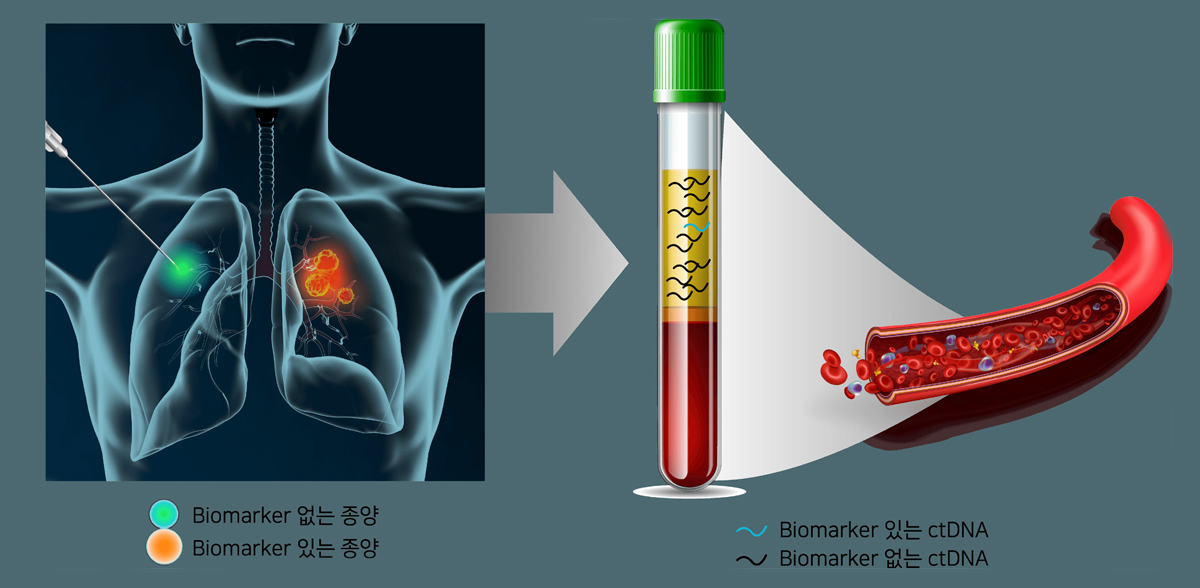 그림1. ctDNA는 미량의 검체에서 target biomarker를 찾을 수 있으며, 조직검사를 보완할 수 있습니다.
그림1. ctDNA는 미량의 검체에서 target biomarker를 찾을 수 있으며, 조직검사를 보완할 수 있습니다.
 그림2. 액체생검을 권고하는 NCCN 임상 진료 가이드라인.
그림2. 액체생검을 권고하는 NCCN 임상 진료 가이드라인.
2. ctDNA 전용 pan-caner panel은 진단과 biomarker 탐색에 적용할 수 있습니다. NGS 유전자패널검사의 고형암 분야는, 2019년 개정(고시 제2019-75호)을 통해, 소규모 암종별 panel에서 대규모 pan-cancer panel로 전환되었습니다. Pan-cancer panel의 유전자 수는 ~500개로 증가되었고, 패널사이즈도 DNA와 RNA를 통합 ~2.5 Mb로 확대되었습니다. 그와 함께, 단일염기치환(SNV)와 삽입/결실(Indel) 외에도 Microsatellite instability(MSI)와 Tumor mutation burden(TMB) 등 biomarker를 탐색하는 Pan-cancer 패널이 출시되고 있습니다.
Biopsy 검체를 활용한 절편길이분석법(fragment analysis) 기반MSI와 whole exome sequencing(WES) 기반 TMB를 NGS 유전자패널검사를 통해 통합분석 하는 방식은 NGS 유전자패널검사의 고형암 분야에 전환점이 되었습니다. 그러나 침습적인 조직검사에 대한 환자 부담과 종양의 각 부위별 상이한 유전변이로 인한 검사 실패율은 여전히 문제로 남아 있습니다.
ctDNA를 활용한 pan-cancer panel로 MSI와 TMB 등 biomarker를 찾는 액체생검 관련 연구가 활발히 진행되고 있습니다.
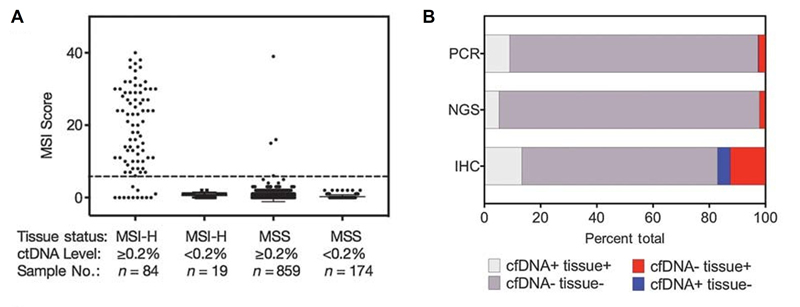 그림3. Concordance of ctDNA MSI status with tissue testing
그림3. Concordance of ctDNA MSI status with tissue testing
 그림4. Comparison of TMB measured by WES (muts/exome) in tissue biopsies and TMB measured from ctDNA (muts/MB), GH: GuardantHealth, FMI: Foundation Medicine.
그림4. Comparison of TMB measured by WES (muts/exome) in tissue biopsies and TMB measured from ctDNA (muts/MB), GH: GuardantHealth, FMI: Foundation Medicine.
| Product Name | NGS Assay | Av. MSI Sites Detected* | Av. Unstable MSI Sies* | Av. MSI Score* | MSI Call |
|---|---|---|---|---|---|
| Seraseq gDNA MSI-High Mix | TSO500 | 106 | 81 | 77.1 | High |
| Seraseq ® FFPE MSI-High RM | TSO500 | 119 | 90 | 75.6 | High |
| 105 | 75 | 71.4 | High |
| TMB Reference Material | Cell Line | TMB Scores (gDNA) | TMB Scores (FFPE) | TMB Scores (ctDNA) |
|---|---|---|---|---|
| Seraseq® TMB Score 7 | Small cell lung cancer; carcinoma | 7.2 ± 0.2 | 7.2 ± 0.4 |
5.6 ± 2.1 (0.5% TF) 10.4 ± 1.7 (2% TF) |
| Seraseq® TMB Score 9 | Lung adenocarcinoma (stage 1) | 9.5 ± 0.4 | 4 7.5 ± 1.3 | N/A |
| Seraseq® TMB Score 13 | B-Lymphocyte | 12.6 ± 0.02 | 12.1 ± 0.3 |
14.1 ± 2.2 (0.5% TF) 20.0 ± 0.9 (2% TF) |
| Seraseq® TMB Score 20 | Non-small cell lung cancer; carcinoma | 20.1 ± 0.2 | 18.6 ± 0.5 |
18.5 ± 2.7 (0.5% TF) 28.1 ± 1.7 (2% TF) |
| Seraseq® TMB Score 26 | Lung adenocarcinoma (stage 4) | 25.8 ± 0.5 | 22.8 ± 3.6 |
14.7 ± 2.4 (0.5% TF) 24.4 ± 1.5 (2% TF) |
표1. SeraSeq MSI, TMB 관련 제품군
3. 액체생검의 취약점과 ctDNA 정도관리물질의 필요성 조직검사 시 채집된 biopsy 검체의 양적, 질적 문제와 마찬가지로 액체생검의 혈액 검체의 적합성은 진단 및추적조사의 유효성과 안전성을 평가하는 중요한 척도입니다.
종양의 병기와 발생위치에 따른 요인 외에도 암종 별로 혈액 내 ctDNA 방출량의 변동성이 크고, 혈액 검체 채집양과 적합한 채혈시간, 보존과 추출 방법에 대한 표준화된 방법이 아직 정립되지 않았습니다. 이런 조건에서 환자 ctDNA 샘플을 활용한 연구와 평가 목적의 검사는 어려울 수밖에 없습니다. 특히, 동등성 평가와 성능 평가와 같이 동일한 검체 시료를 사용해야 하는 경우에는 적은 양의 환자 ctDNA를 활용하는 것이 현실적으로 불가능 합니다.
| AKT1 | EGFR | NCOA4-RET |
| ALK | ERBB2 | CD74-ROS1 |
| BRAF | KIT | EML4-ALK |
| BRCA1 | KRAS | |
| BRCA2 | PIK3CA |
표2. 환자검체 유사 reference material 에 포함된 13개의 유전자
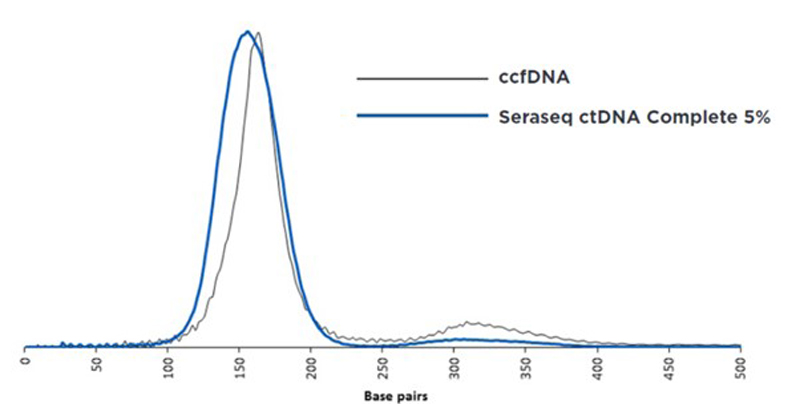 그림5. 환자 검체의 ctDNA 패턴과 SeraSeq ctDNA 정도관리 물질의 패턴 유사성
그림5. 환자 검체의 ctDNA 패턴과 SeraSeq ctDNA 정도관리 물질의 패턴 유사성
대안으로 patient-like reference material(이하, reference material) 사용을 검토해 볼 수 있습니다.
Seraseq ctDNA Complete reference materials는 NGS기반의 ctDNA 검사를 철저하게 검증하고 임상적으로 빠르게 적용할 수 있도록 특별히 고안되었습니다. 이러한 직교적으로 검증된 truth-set 물질은 단일 표준물질에 여러 변이의 유형들을 거의 완벽하게 커버함으로써 검사에 대한 검증 기간을 수주에서 많게는 수개월까지 단축시킬 수 있습니다. 검사의 다양성을 위해 0%부터 0.1%, 0.5%,1% 2.5%, 5%까지 다양한 allele frequency를 제공합니다.
| Product | Material No | Conc. | Fill Volume | Total Mass |
|---|---|---|---|---|
| Seraseq ctDNA MRD Panel Mix (Kit contains 4 vials: 0%, 0.5%, 0.05% & 0.005% turnor fractions) | 0710-2146 | 10 ng/ul | 20 ul | 200 ng (X4) |
| BCL2 | MYD88 | SF3B1 | HSP90AA1-BCL6 |
| BRAF | CXCR4 | STAT3 | CCND1-CDC42BPB |
| DNMT3A | NOTCH1 | STAT5B | BIRC3-MALT1 |
| EZH2 | NOTCH2 | TP53 | MYC-IGH |
| IDH2 | RHOA | NPM1-ALK | TBL1XR1-TP63 |
표3. Seraseq ctDNA 제품정보
# Reference
1. NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines) Version 3.2021: Non-Small Cell Lung Cancer
2. NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines) Version 1.2021: Breast Cancer
3. NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines) Version 1.2021: Esophageal and Esophagogastric Junction Cancers
4. NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines) Version 1.2021: Gastric Cancer
5. NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines) Version 2.2021: Prostate Cancer
6. NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines) Version 2.2021: Pancreatic Adenocarcinoma
7. NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines) Version 2.2021: Histiocytic Neoplasms
8. Aggarwal C, Thompson JC, Black TA, et al. Clinical Implications of Plasma-Based Genotyping With the Delivery of Personalized Therapy in Metastatic Non-Small Cell Lung Cancer. JAMA Oncol. 2019;5(2):173-180. doi:10.1001/jamaoncol.2018.4305
9. Leighl NB, Page RD, Raymond VM, et al. Clinical Utility of Comprehensive Cell-free DNA Analysis to Identify Genomic Biomarkers in Patients with Newly Diagnosed Metastatic Non-small Cell Lung Cancer. Clin Cancer Res. 2019;25(15):46914700. doi:10.1158/1078-0432.CCR-19-0624
10. Palmero R, Taus A, Viteri S, et al. Biomarker Discovery and Outcomes for Comprehensive Cell-Free Circulating Tumor DNA Versus Standdard-of-Care Tissue Testing in Advanced Non-Small Cell Lung Cancer. JCO Precision Oncology. 2021; 5:93-102. doi:10.1200/PO.20.00241
11. Sholl LM, Do K, Shivdasani P, et al. Institutional implementation of clinical tumor profiling on an unselected cancer population. JCI Insight. 2016;1(19): e87062. Published 2016 Nov 17. doi: 10.1172/jci.insight.87062
12. Meric-Bernstam F, Brusco L, Shaw K, et al. Feasibility of Large-Scale Genomic Testing to Facilitate Enrollment Onto Genomically Matched Clinical Trials. J Clin Oncol. 2015;33(25):2753-2762. doi:10.1200/JCO.2014.60.4165

